Nicole Marie Kahn1 ID· Mayra Florencia Defanti2 ID· Yanina Gabriela Carlino1 ID
1Servicio de Gastroenterología y Endoscopia.
2Servicio de
Anatomía Patológica.
Hospital Privado Universitario de Córdoba. Provincia de Córdoba.
Argentina.
Acta Gastroenterol Latinoam 2026;56(1):102-106
Recibido: 19/04/2025 / Aceptado: 12/03/2026 / Publicado online el 31/03/2026 / https://doi.org/10.52787/agl.v56i1.484
Antecedentes. La ecoendoscopía es una técnica diagnóstica mínimamente invasiva que combina imágenes endoscópicas y ultrasonográficas para evaluar lesiones gastrointestinales y tejidos adyacentes. Este reporte describe su uso en el diagnóstico de metástasis mesorrectales de carcinoma de células claras renales. Presentación del caso. Mujer de 54 años con antecedentes de carcinoma de células claras renales tratado con nefrectomía derecha. En la tomografía de control presentó engrosamiento parietal rectal y nódulos mesorrectales. La ecoendoscopía identificó una lesión subepitelial rectal y nódulos mesorrectales, y la biopsia guiada confirmó metástasis de carcinoma de células claras renales (PAX8 y CD10 positivas). Conclusión. La ecoendoscopía es un método efectivo para diagnosticar metástasis mesorrectales y se destaca por su utilidad en casos infrecuentes como metástasis de carcinoma de células claras renales.
Palabras claves. Ecoendoscopía, carcinoma de células claras renales, metástasis mesorrectal, diagnóstico mínimamente invasivo, reporte de un caso.
Background. Endoscopic ultrasound is a minimally invasive diagnostic technique that combines endoscopic and ultrasonographic imaging to evaluate gastrointestinal and adjacent tissue lesions. This report describes its use in the diagnosis of mesorectal metastases from renal clear cell carcinoma. Case Presentation. A 54-year-old woman with a history of renal clear cell carcinoma treated with right nephrectomy. Follow-up computed tomography revealed rectal wall thickening and mesorectal nodules. Endoscopic ultrasound identified a subepithelial rectal lesion and mesorectal nodules, and guided biopsy confirmed metastases from renal clear cell carcinoma (PAX8 and CD10-positive). Conclusion. Endoscopic ultrasound is an effective method for diagnosing mesorectal metastases, and is particularly useful in rare renal clear cell carcinoma cases.
Keywords. Endoscopic ultrasound, renal clear cell carcinoma, mesorectal metastases, minimally invasive diagnosis, case report.
Abreviaturas
USE: Ultrasonografía endoscópica.
CCCR: Carcinoma de células claras renales (Renal
Clear Cell Carcinoma).
TC: Tomografía computarizada (Computed Tomography).
RM:
Resonancia magnética (Magnetic Resonance Imaging).
PAAF: Punción aspirativa con aguja fina (Fine
needle aspiration).
GIST: Tumor estromal gastrointestinal (Gastrointestinal Stromal Tumor).
La USE es una técnica diagnóstica que integra ultrasonografía de alta resolución y endoscopía para evaluar lesiones en el tracto gastrointestinal y estructuras adyacentes. Es ampliamente utilizada para estadificar lesiones malignas, caracterizar lesiones submucosas y guiar biopsias por aspiración con aguja fina.1 - 3 En el contexto de patologías rectales, la USE y la RM son técnicas complementarias con indicaciones específicas. La USE ofrece mayor precisión para la evaluación de las capas de la pared rectal y es superior en la estadificación de tumores tempranos (T1-T2), con sensibilidad del 87,8% y especificidad del 98,3% para lesiones T1.4, 5 Por su parte, la RM permite evaluar estructuras mesorrectales, la fascia mesorrectal y el margen de resección circunferencial, con especificidad del 94% para la planificación quirúrgica.6, 7
El CCCR representa el 75-80% de los cánceres renales y es conocido por metastatizar a sitios distantes como pulmones (70%), ganglios linfáticos (45%), huesos (32%), hígado (18%), glándula suprarrenal (10%) y cerebro (8%).8 Sin embargo, las metástasis mesorrectales son excepcionalmente raras, con escasos casos reportados.9 - 11 Este reporte presenta un caso de metástasis mesorrectal de CCCR diagnosticada por USE y destaca la utilidad de esta técnica en un escenario clínico infrecuente. Asimismo, enfatiza su relevancia en la estadificación y el manejo oncológico.
Mujer de 54 años con antecedentes de CCCR diagnosticado hace 4 años, tratada con nefrectomía total derecha. La paciente se presentó para seguimiento oncológico de rutina anual. Una TC reveló un engrosamiento focal hipervascularizado de la pared rectal inferior (23 mm de diámetro anteroposterior, 12 mm transversal) y dos nódulos mesorrectales: uno de 22 mm x 28 mm en la posición de las 2 en punto, en contacto con la pared rectal, y otro de 14 mm x 9 mm en la posición de las 3 en punto, íntimamente relacionado con la fascia mesorrectal. Estos hallazgos suscitaron la sospecha de neoplasia primaria rectal con diseminación regional, GIST o metástasis.
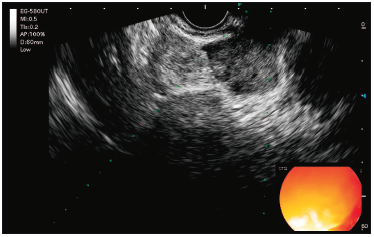
Se realizó una colonoscopía que identificó una lesión subepitelial rectal. La USE subsiguiente reveló una lesión subepitelial en el recto medio-inferior, de aproximadamente 10 mm x 15 mm, originada en la cuarta capa ecogénica (muscular propia), continua con una formación nodular mesorrectal de 21 mm x 15 mm. También se observaron ganglios linfáticos mesorrectales regionales de 5 mm a 6 mm (Figura 1 y 2).
Figura 1. Lesión originada en la cuarta eco capa (muscular propia) en
mesorrecto

Figura 2. Formación subepitelial de 10 x 15 mm continua con lesión nodular de 21 x 15
mm en mesorrecto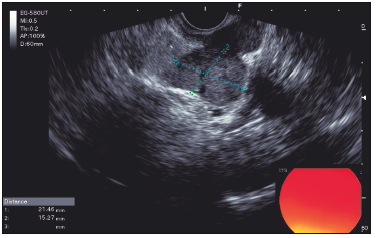
Se realizó una biopsia guiada por USE utilizando un equipo lineal FujiFilm Ultrasonic Endoscope EG-580UT con biopsia con aguja fina (FNB) de calibre 19 (Acquire, Boston Scientific). Se efectuaron 5 pases con técnica de movimiento de fanning bajo guía ultrasonográfica continua y se obtuvo material suficiente para las evaluaciones citológica e histopatológica. No se observaron complicaciones inmediatas relacionadas con el procedimiento.
La biopsia guiada por USE fue complementada con una evaluación citológica rápida onsite (ROSE), la cual mostró citología positiva para malignidad en el primer pase. Posteriormente, la histopatología diferida confirmó células claras con inmunohistoquímica positiva para PAX8 y CD10, consistente con metástasis de CCCR (Figuras 3 y 4).
Figura 3. Fragmento de biopsia de lesión mesorrectal con tinción CD10 de membranas
compatible con células claras renales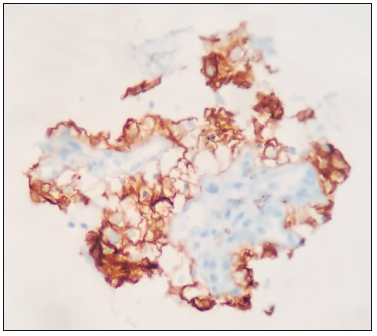
Figura 4. Fragmento de biopsia de lesión mesorrectal con tinción PAX8 de núcleos
compatible con células claras renales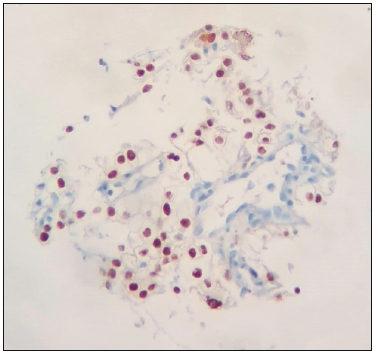
Tras la confirmación diagnóstica, la paciente fue derivada al equipo oncológico multidisciplinario. Dado el carácter metastásico único u oligometastásico y el buen estado funcional, se consideró el inicio de terapia sistémica dirigida con inmunoterapia con Nivolumab y luego control imagenológico para reevaluación oncológica.
Al momento de este reporte, la paciente permanecía asintomática y en evaluación para determinar el plan quirúrgico a realizar. No se reportaron complicaciones asociadas al procedimiento de USE.
La metástasis mesorrectal de CCCR es una entidad clínica poco común, con informes
limitados en la literatura y, por lo tanto, representa un desafío diagnóstico. Las metástasis
gastrointestinales del CCCR representan solo el 1,6% de todos los casos de CCCR metastásico, siendo las
localizaciones más frecuentes el estómago y el duodeno, mientras que las metástasis rectales son
excepcionalmente raras.10 - 12 El CCCR tiende a metastatizar por vía hematógena, y la latencia
entre el tratamiento inicial y la aparición de metástasis es bien conocida, con un intervalo medio de 5,4
años desde el diagnóstico de CCCR.10, 13
El mesorrecto, con su rica vascularización y
drenaje linfático, puede ser un sitio metastásico inusual, pero su identificación precisa es crucial para la
estadificación.12 El diagnóstico diferencial en este caso incluía adenocarcinoma rectal primario,
GIST u otras enfermedades metastásicas, lo que requirió un diagnóstico tisular para su posterior
confirmación.14
La USE ha demostrado una precisión diagnóstica del 85-95% en lesiones rectales y perirrectales, con sensibilidad del 87,8% y especificidad del 98,3% para tumores T1, y una tasa de complicaciones inferior al 1%.1, 4, 5 En este caso, la USE permitió caracterizar la lesión, identificar su extensión mesorrectal y obtener tejido para un diagnóstico definitivo, evitando procedimientos quirúrgicos más invasivos.12 Estudios previos han descrito metástasis rectales de CCCR diagnosticadas por resección quirúrgica, pero la USE ofrece una alternativa menos invasiva con resultados comparables.10, 12, 16 La inmunohistoquímica (PAX8, CD10) fue fundamental para confirmar el origen renal, en concordancia con criterios diagnósticos establecidos que indican que PAX8 tiene una sensibilidad del 83-100% para CCCR y CD10 del 76-85%.17
En pacientes con metástasis rectal o mesorrectal de CCCR, el manejo debe ser individualizado. La resección quirúrgica local puede ser curativa en metástasis solitarias u oligometastásicas, mientras que la terapia sistémica constituye el pilar en la enfermedad diseminada o de alto volumen.18 La detección temprana mediante la USE permite una intervención oportuna y potencialmente metastásica-dirigida.
La serie más grande reportada corresponde al estudio multicéntrico GETUG (2024), que identificó a 74 pacientes con 87 metástasis gastrointestinales de CCCR, siendo las localizaciones más frecuentes el estómago (50%) y el duodeno (41,6%), y con solo casos aislados de afectación rectal.9 El intervalo medio entre el diagnóstico de CCCR y la aparición de metástasis gastrointestinales fue de 5,4 años, y la supervivencia media fue de 19 meses.
Los casos específicos de metástasis rectales reportados en la literatura incluyen el
de Rosito y col. (2002), quienes describieron el primer caso documentado en el que la metástasis se presentó
9 meses después de la nefrectomía; el de Zheng y col. (2017), en el cual la metástasis rectal
postnefrectomía se manifestó a los 10 años; y el de Zygomalas y
col. (2020), en el que la metástasis a la fosa isquiorrectal se presentó 17 años después del tratamiento
inicial.10, 12, 13
Una revisión sistemática de Janjic y col. (2022) analizó 162 pacientes
con metástasis rectales de diversos orígenes primarios e identificó
solo casos aislados de CCCR como origen, confirmando así su rareza excepcional.14
Estos casos confirman que las metástasis rectales/mesorrectales de CCCR típicamente ocurren años después de la nefrectomía (rango: 9 meses a 17 años), requieren alto índice de sospecha clínica y confirmación histológica con inmunohistoquímica, y representan menos del 2% de todas las metástasis de CCCR.9 - 11
El presente caso contribuye a esta escasa literatura al destacar la utilidad de la USE - PAAF como método diagnóstico mínimamente invasivo para esta infrecuente presentación clínica.
El enfoque multidisciplinario aseguró un manejo integral del paciente.
Limitaciones: La infrecuencia de la metástasis mesorrectal de carcinoma de células claras renales dificulta el análisis comparativo debido a la escasez de casos similares.
Relevancia clínica: Este caso resalta la importancia de considerar metástasis atípicas en pacientes con antecedentes de carcinoma de células claras renales y el valor de la USE en el diagnóstico de lesiones mesorrectales.
La biopsia guiada por USE es una herramienta diagnóstica efectiva y mínimamente invasiva para las metástasis mesorrectales. Su capacidad para proporcionar imágenes detalladas y muestreo tisular dirigido la hace esencial en escenarios oncológicos complejos, especialmente para patrones metastásicos raros. Se debe considerar la USE en la evaluación diagnóstica de lesiones mesorrectales sospechosas, particularmente en pacientes con antecedentes de neoplasias propensas a diseminación metastásica atípica.
Consentimiento para la publicación. Para la confección de este manuscrito, se utilizaron datos anonimizados que no han distorsionado su significado científico.
Propiedad intelectual. Los autores declaran que los datos y las figuras presentes en el manuscrito son originales y se realizaron en las instituciones a las que pertenecen.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflicto de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor

© 2026 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Kahn N M, Defanti M F y Carlino Y G. Biopsia guiada por ecoendoscopía como herramienta diagnóstica mínimamente invasiva para metástasis mesorrectal de carcinoma de células claras renales: reporte de caso. Acta Gastroenterol Latinoam. 2026;56(1):102-106. https://doi.org/10.52787/agl.v56i1.484
Correspondencia:
Nicole Marie Kahn
Correo electrónico: nickykahn98@gmail.com
Acta Gastroenterol Latinoam 2026;56(1):102-106