Cecilia Zubiri1 ID· Anabella Zosi1 ID· Román Bigliardi2 ID
1Servicio de Gastroenterología del Hospital de Niños Sor María Ludovica de La
Plata.
2Jefe del Servicio de Gastroeterología pediátrica del Hospital
Posadas
Provincia de Buenos Aires. Argentina.
Acta Gastroenterol Latinoam 2026;56(1):41-56
Recibido: 04/12/2025 / Aceptado: 09/03/2026 / Publicado online el 31/03/2026 /
https://doi.org/10.52787/agl.v56i1.576
El estreñimiento funcional refractario es un desafío persistente en pediatría. Más allá del polietilenglicol y los laxantes tradicionales, surgen nuevas terapias farmacológicas y no farmacológicas. Entre los medicamentos innovadores se destacan los agentes prosecretorios, como linaclotida (aprobada para mayores de 6 años), lubiprostona y plecanatida, que aumentan la secreción intestinal. Otros fármacos, como prucaloprida (agonista 5HT-4) y piridostigmina, buscan mejorar la motilidad. Las terapias rectales e intervencionistas incluyen la irrigación transanal -que muestra buenos resultados-, los enemas anterógrados y la inyección de toxina botulínica A, útiles para disfunciones específicas. La biorretroalimentación sigue siendo una herramienta efectiva. La neuromodulación se posiciona como una opción prometedora. La estimulación del nervio sacro implantada y las técnicas no invasivas como la estimulación percutánea/transcutánea del nervio tibial posterior y la neuroestimulación transcutánea sacra, demuestran mejoras en los síntomas y la calidad de vida. Existen terapias poco exploradas pero prometedoras a futuro como la cápsula vibratoria, la neuroestimulación magnética y los enfoques mente-cuerpo como la hipnosis. Es crucial la investigación pediátrica específica y un enfoque individualizado del tratamiento para optimizar la adherencia y los resultados en estos pacientes complejos.
Palabras claves. Estreñimiento funcional refractario, pediatría, incontinencia fecal, laxantes, irrigación transanal, neuroestimulación sacra y tibial posterior, toxina botulínica.
Refractory functional constipation is a persistent challenge in pediatrics. Beyond polyethylene glycol and traditional laxatives, new pharmacological and non-pharmacological therapies are emerging. Among the innovative medications, prosecretory agents like linaclotide (already approved for children over 6 years old), lubiprostone and plecanatide, wich increase intestinal secretion, stand out. Other drugs, such as prucalopride (5HT-4 agonist) and pyridostigmine, aim to improve motility. Rectal and interventional therapies include transanal irrigation, -which has shown good results-; antegrade enemas and botulinum toxin A injections, which are useful for specific dysfunctions. Biofeedback remains an effective tool. Neuromodulation is emerging as a promising option. Implanted sacral nerve stimulation and non-invasive techniques such as percutaneous/transcutaneous tibial nerve stimulation and transcutaneous sacral neuromodulation demonstrate improvements in symptoms and quality of life. There are therapies that have been little explored but show promise for the future, such as vibrating capsules, magnetic neurostimulation, and mind-body approaches like hypnosis. Specific pediatric research and an individualized treatment approach are crucial to optimize adherence and outcomes in these complex patients.
Keywords. Refractory functional constipation, pediatrics, fecal incontinence, laxatives, transanal irrigation, sacral and posterior tibial nerve stimulation, botulinum toxin.
Abreviaturas
EF: Estreñimiento funcional.
PEG: Polietilenglicol
ESPGHAN: Sociedad
Europea de Gastroenterología, Hepatología y Nutrición Pediátrica.
NASPGHAN: Sociedad
Norteamericana de Gastroenterología, Hepatología y Nutrición Pediátrica.
FDA: Food and Drug
Administration.
ITA: Irrigación transanal.
ITB: Inyección de toxina
botulínica.
MAR: malformación ano rectal.
MMC: Mielomeningocele.
ENS:
Estimulación del nervio sacro.
ENTP: Estimulación del nervio tibial
posterior.
ETNTP: Estimulación transcutánea del nervio tibial posterior.
EPNTP: Estimulación percutánea del nervio tibial posterior.
EET:
Estimulación eléctrica transcutánea abdominal.
El estreñimiento funcional (EF) es frecuente en pediatría (hasta 9,5%).1 Su diagnóstico se basa en los criterios de Roma IV según síntomas y edad (Tabla 1).2-3 Los síntomas habituales son deposiciones grandes, dolorosas, poco frecuentes, con o sin dolor abdominal e incontinencia.1 El EF se clasifica en tránsito normal, tránsito lento y alteración defecatoria, esta última por retención fecal, siendo muy común en niños.4
Tabla 1. Criterios de Roma IV para estreñimiento funcional en pediatría
El manejo inicial es no farmacológico. Se basa en la ingesta normal de fibra y líquidos, actividad física y pautas educativas para el paciente y su familia.5-6 Desde los 4 años se tiene en cuenta el control del esfínter anal.5-6 Algunos pacientes no responden al tratamiento mencionado y requieren la incorporación de fármacos. El polietilenglicol (PEG) es la primera opción terapéutica, pudiendo asociarse a laxantes estimulantes en los casos más complejos. Hasta un 40% de los niños no responden a estas terapias. El estreñimiento intratable o refractario es el que no mejora tras 3 meses de tratamiento óptimo. En estos casos se solicitan estudios adicionales ante la sospecha de una causa orgánica.6 (Gráfico Algoritmo 1) Existen muchas alternativas terapéuticas farmacológicas y no farmacológicas , las cuales se resumen en la Tabla 2 y se detallan en esta revisión.7-9
Algoritmo de manejo del estreñimiento funcional en pediatría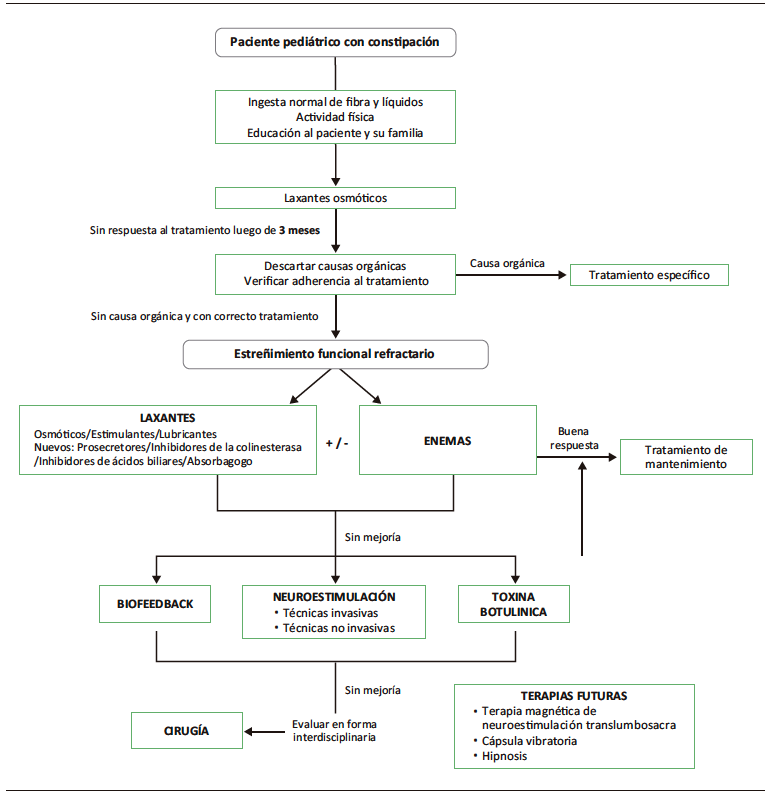
Tabla 2. Agentes farmacológicos y terapias estándar para el manejo del estreñimiento
funcional en niños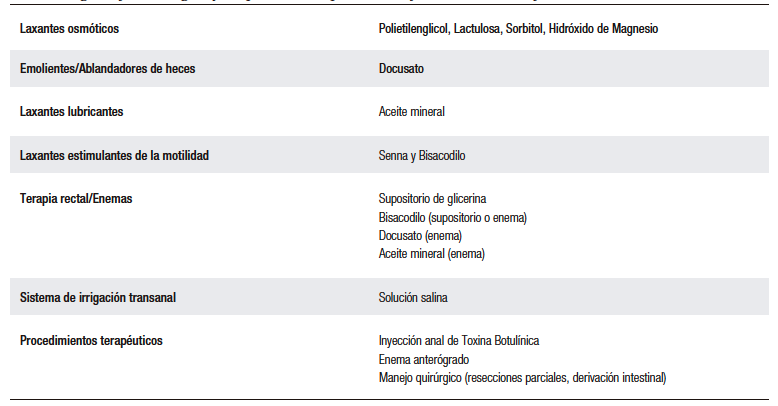
Terapias farmacológicas
Polietilenglicol
Las guías de las Sociedades Europea y Norteamericana de Gastroenterología, Hepatología y Nutrición Pediátrica (ESPGHAN/NASPGHAN) recomiendan PEG como primera opción cuando falla el manejo no farmacológico.6 La dosis es 0,2 - 0,8 g/kg/día (inicial 0,4 g/kg/día), ajustada según la respuesta.6 Sus efectos adversos son leves: distensión, flatulencias, náuseas y dolor abdominal.5, 10
Laxantes osmóticos alternativos
Como segunda línea de tratamiento, en caso de no contar con PEG, se utiliza lactulosa.7 El hidróxido de magnesio es menos efectivo y tolerado que el PEG.8 En lactantes alimentados con fórmulas ricas en magnesio, las heces son más blandas y frecuentes que con la fórmula estándar.
Laxantes estimulantes
Se indican como segunda línea cuando los laxantes osmóticos no son suficientes.7 Incluyen a los difenilmetanos (bisacodilo, picosulfato) y a las antraquinonas (sen), que aumentan la motilidad colónica.4,11 Pueden causar cólicos y dolor abdominal. Son seguros a corto y largo plazo.11,12 El uso prolongado de senósidos puede producir melanosis coli, sin repercusión clínica.13
Lubricantes
Ablandan o lubrican las heces. El más usado es el aceite mineral (parafina líquida); seguro y con buenos resultados en EF, aunque la evidencia es limitada.5,14,10 Puede causar dolor abdominal, náuseas, vómitos y flatulencias, generalmente leves.4,5,10 Su uso prolongado disminuye la absorción de las vitaminas liposolubles.15
Alternativas terapéuticas farmacológicas y no farmacológicas
Actualmente disponemos de nuevas terapias, con mayor y mejor evidencia en la población adulta ya que los primeros estudios se realizan en ellos.
Agentes prosecretores
Aumentan la secreción intestinal y aceleran el tránsito.
Lubiprostona
Activa los canales de cloro e incrementa la secreción intestinal.16 Su uso fue aprobado por la FDA (Food and Drug Administration) para adultos.17 En niños mayores de 6 años muestra una eficacia y seguridad variables.18 - 19
Linaclotida
Activa la guanilato ciclasa-C y aumenta la secreción luminal. Es el primer fármaco aprobado por la FDA para el EF pediátrico en niños mayores de 6 años. La dosis es 72 mcg/día. Está contraindicada en niños menores de 2 años.20 - 21
Plecanatida
Es agonista de la guanilato ciclasa-C. Eficaz y segura en adultos,22-26 no tiene datos pediátricos publicados. En estudios preclínicos produjo mortalidad en ratones jóvenes. Existe un ensayo pediátrico en curso.
Agonistas 5HT-4
Estimulan la liberación de acetilcolina, aumentan la motilidad y la secreción.
La más utilizada es prucaloprida.4 Fue aprobada por la FDA para su uso en adultos, con buena eficacia y seguridad.27-28 Está indicada cuando se sospecha tránsito lento o dismotilidad colónica/gastrointestinal. En el estreñimiento intratable se encontraron resultados pediátricos variables, sin clara superioridad frente al placebo.29-32 Las diferencias fisiopatológicas adulto-niño explican su menor eficacia pediátrica.
Inhibidor de colinesterasa
Piridostigmina
Aumenta la acetilcolina, mejorando la motilidad.33 Existen datos limitados en adultos33-34 y solo reportes de casos en niños. No cuenta con evidencia concluyente en el EF pediátrico.35-36
Ácidos biliares
Elobixibat
Inhibe la reabsorción ileal de los ácidos biliares, aumentando su efecto osmótico y la motilidad colónica.37 Es eficaz y seguro en adultos.38-39 Aún no se cuenta con datos pediátricos.
Absorbagogo
Tenapanor
Previene la reabsorción de líquido colónico al inhibir el intercambiador de Na(+)/H(+),40 reduciendo la absorción de sodio. Fue aprobado por la FDA para el tratamiento del síndrome de intestino irritable con estreñimiento en adultos. Su efecto adverso principal es la diarrea.41 Sin evidencia actual en pediatría.
Enemas e irrigación transanal
Cuando la terapia laxante oral estándar no alivia los síntomas, se puede considerar la terapia adyuvante rectal, con enemas o con irrigación transanal (ITA).6
Enemas
Existen varios tipos de enemas para facilitar la eliminación rectal de las heces. Los más utilizados son los de cloruro de sodio, fósforo sódico o aceite mineral. El docusato sódico puede prepararse como un enema de pequeño volumen, actúa ablandando y lubricando las heces. Se utilizan en la primera etapa del tratamiento en niños que consultan por impactación fecal y encopresis secundaria. Forman parte del programa de manejo intestinal en los niños con malformaciones anorrectales e intestino neurogénico.4
Sistema de irrigación transanal
La ITA consiste en introducir agua a través del ano, en el recto y el colon distal, con un volumen de 10 a 20 ml/kg, para prevenir la acumulación de heces. El sistema de irrigación anal Peristeen® (Coloplast A/S, Kokkedal, Dinamarca o Mallinckrodt, St. Louis, MO) (Figuras 1 y 2) cuenta con un catéter endo rectal con un balón insuflable en su extremo distal, que impide la salida del líquido hacia el exterior mientras se realiza el lavado. Al terminar de pasar todo el líquido indicado, se desinfla el balón y se retira el catéter, dando lugar a la evacuación de heces hidratadas.42 Este sistema otorga independencia a los pacientes que deben utilizar esta terapéutica de manera crónica.
Figura 1. Irrigador ano rectal Peristeen®
Plus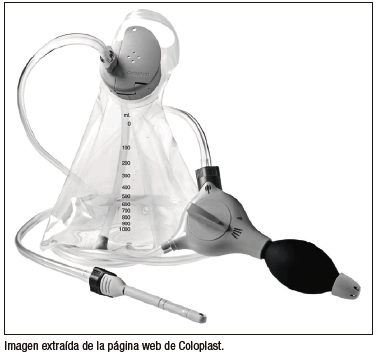
Figura 2. Catéter del irrigador posicionado en el recto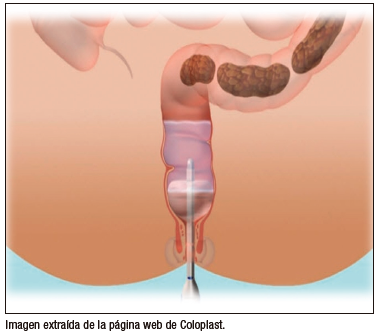
El uso del ITA ha sido muy estudiado en programas de manejo intestinal para los niños con malformaciones recto anales e intestino neurogénico.43-44 En niños con EF demostraron buenos resultados, con un rango de entre 41% y 73% de efectividad y mejoras en la calidad de vida.42-48
Las complicaciones severas son extremadamente infrecuentes e incluyen sangrado rectal significativo y perforación intestinal (0,002%).49-51 Las complicaciones menores incluyen fugas alrededor del balón, dolor abdominal durante la administración del líquido y ruptura del balón.46, 47, 51
Enema Anterógrado
Puede considerarse en EF o incontinencia fecal refractaria a todo tratamiento médico indicado. Se trata de una cirugía mínimamente invasiva, donde se coloca un botón de cecostomía (Figura 3).
Generalmente la respuesta es buena y mejora la calidad de vida del paciente. Actualmente su uso es limitado, dada la gran oferta de tratamientos previos existentes con buenos resultados.
Las complicaciones son menores pero frecuentes, como fugas periestomales, infección y estenosis del ostoma, cateterización difícil con riesgo de crear un conducto falso y contaminación persistente.52-55 Un estudio informó que el 10 % de los niños necesitaron reoperarse.52 No existen datos previos predictores de buena respuesta, pero la utilización del enema retrógrado preoperatorio con buena respuesta podría ser un posible parámetro.56
Figura 3. Botón para enemas anterógrados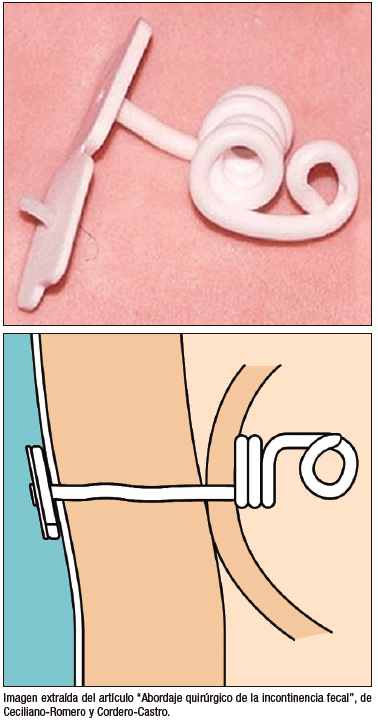
Inyección de toxina botulínica
La inyección de toxina botulínica A (ITB) en el esfínter anal fue descrita inicialmente por Langer en 1997 para disminuir los síntomas obstructivos en niños con enfermedad de Hirschsprung.57
No existe un consenso en su técnica de aplicación. Se puede aplicar en dos o cuatro cuadrantes, con o sin guía ecográfica (Figura 4).58 Actualmente está indicada en los trastornos pediátricos de la defecación como disinergia defecatoria, en niños con malformaciones anorrectales (MAR), dismotilidad colónica, acalasia del esfínter anal interno y EF.59-62
Figura 4. Técnica de aplicación de toxina botulínica en el esfínter anal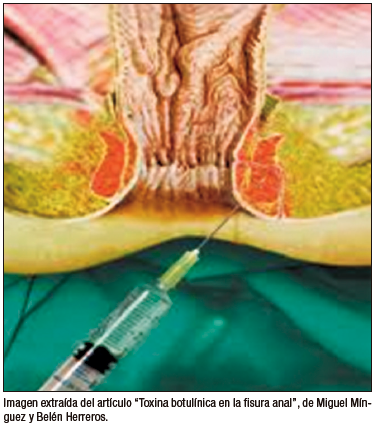
Los efectos secundarios de la ITB generalmente son leves. La incontinencia fecal y/o urinaria los primeros días o semanas posteriores a la inyección, son el evento adverso más frecuente y se autolimitan.59, 60, 63 En un estudio que comparó la efectividad de la IBT frente a la implementación de un programa de manejo intestinal con utilización de senósidos en pacientes con EF y obstrucción al tracto de salida, no encontró diferencias significativas entre ambos grupos, pero el número de pacientes fue escaso.64
Bioretroalimentación (Biofeedback)
Técnica descripta en 1974 por Engel BT y colaboradores,65 consiste en colocar una sonda con un balón en su extremo distal en el orificio anal, que se insufla una vez adentro del recto simulando la llegada de materia fecal. El niño va observando todo en una pantalla, que puede tener dibujos animados que responden a los cambios de presiones (Figura 5). Se solicita al niño que haga ejercicios de pujo y contracción que va aprendiendo mediante retroalimentación visual y verbal a medida que se intenta ir produciendo algún grado de sensibilidad rectal. Es eficaz para controlar los trastornos del suelo pélvico y para mejorar la función anorrectal.66-70
Figura 5. Programa de biorretroalimentación para niños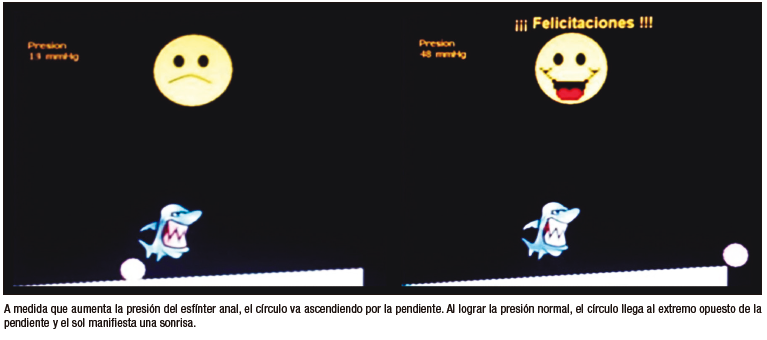
En los Hospitales Posadas y Sor María Ludovica de Argentina se trataron 157 pacientes; 42 con EF refractario, 71 con mielomeningocele (MMC) y 44 con MAR (datos no publicados). El 58,6% logró la continencia total, un 20,4% continencia parcial y un 21% no mejoró. Los mejores resultados se observaron en pacientes con MMC y MAR. Los niños con EF refractario fueron los de peor evolución.
Neuroestimulación/Neuromodulación
Se puede realizar con diferentes técnicas:
Técnicas invasivas
• Electroestimulación del nervio sacro con catéter
implantable quirúrgicamente.
• Electroestimulación percutánea del nervio tibial
posterior.
Técnicas no invasivas
• Electroestimulación transcutánea del nervio tibial
posterior.
• Electroestimulación transcutánea del nervio
sacro.
• Electroestimulción interferencial transcutánea
abdominal.
• Terapia magnética de neuroestimulación trans-
lumbosacra.
Estimulación del nervio sacro con dispositivo implantado quirúrgicamente
Actualmente se considera la alternativa de neuromodulación más estudiada y consolidada para el tratamiento de los trastornos defecatorios en adultos. Consiste en la aplicación de estimulación eléctrica de baja amplitud a la raíz nerviosa sacra mediante un cable implantado quirúrgicamente a través del foramen sacro y conectado a un generador de pulsos y a una batería implantados en el glúteo.71 La implantación permanente puede realizarse tras demostrar su eficacia mediante estimulación temporal con un generador de pulsos externo) (Figura 6).72
Figura 6. Terapias de neuromodulación disponibles para el estreñimiento funcional en
niños4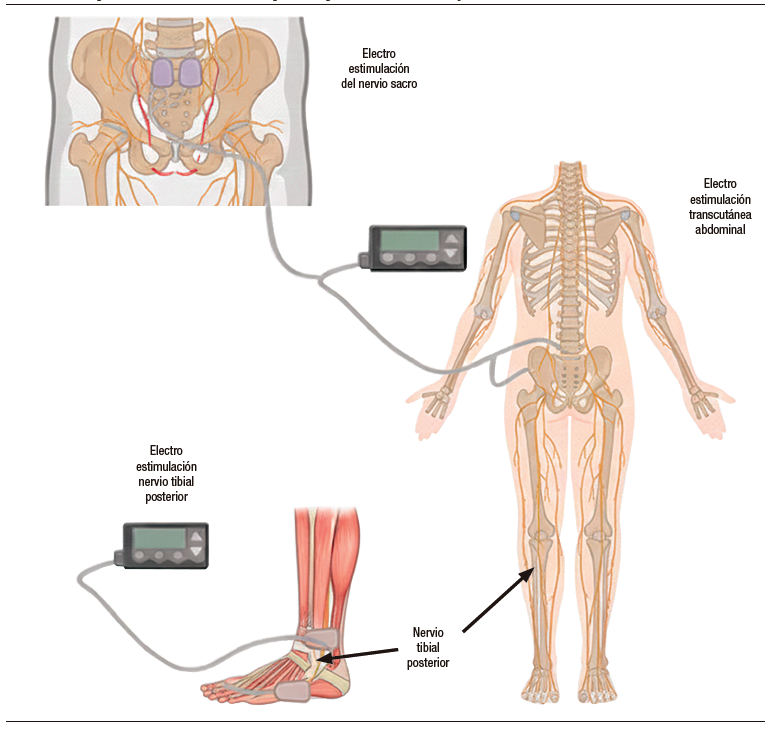
La estimulación del nervio sacro (ENS) es útil en el tratamiento de la incontinencia fecal, el estreñimiento y la incontinencia urinaria. Se cree que actúa mediante la modulación y estimulación de vías centrales, autónomas, del sistema nervioso entérico u otras vías. Aumenta la frecuencia de las contracciones colónicas de alta amplitud propagadas en adultos con estreñimiento de tránsito lento4, 73, 74 y mejora la sensibilidad, como se ha demostrado por manometría recto anal.73-75
La FDA aprobó su indicación en población adulta con incontinencia fecal y/o urinaria. No hay suficiente evidencia en pediatría.76 Sin embargo, existen múltiples estudios que indican que la ENS puede ayudar en el manejo del EF pediátrico, mejorando los síntomas de estreñimiento en el 70-80% de los casos, como así también la calidad de vida.77-81
Se realizaron estudios comparativos entre ENS y enema anterógrado. Se encontró que los niños sometidos a ENS experimentaron menos ensuciamiento intestinal, mientras que los niños con enema anterógrado mejoraron la frecuencia de las deposiciones, la interrupción del tratamiento con laxantes y el dolor abdominal.82
Un estudio prospectivo incluyó adolescentes que continuaban presentando síntomas de estreñimiento a pesar del uso de enema anterógrado y les ofrecieron realizar ENS, logrando cerrar la cecostomía a los 2 años en un 45% de los casos.83
Park y col.84 estudiaron 65 pacientes pediátricos en los que se implementó ESN con dispositivos implantados quirúrgicamente. Observaron una mejora significativa de la incontinencia fecal. Los niños con trastornos orgánicos de base tuvieron menor respuesta que aquellos con trastornos funcionales. El 94% de los pacientes reportó mejoría y aseguró que repetiría su decisión de iniciar la ENS.
Si bien la ENS es una terapia prometedora para el manejo del estreñimiento refractario en pediatría, se reportaron eventos adversos frecuentes con la colocación del dispositivo.4 Entre ellos se destacan la necesidad de retirar el dispositivo por razones como el desplazamiento del electrodo, la infección de la herida en el sitio del electrodo o del generador, y el mal funcionamiento del dispositivo. Las tasas de explantación del dispositivo oscilaron entre el 18% y el 56%; algunas fueron seguidas de reimplantación.79, 82, 83, 85
Estimulación percutánea y transcutánea del nervio tibial posterior
La estimulación del nervio tibial posterior (ENTP) es otra terapia neuromoduladora novedosa que consiste en aplicar estimulación eléctrica al nervio tibial posterior a la altura del tobillo, ya sea de forma percutánea con una aguja (EPNTP) o transcutánea con dos electrodos adheridos a la piel (ETNTP) (Figura 6).4
Se cree que esta estimulación del nervio tibial, una rama distal del nervio ciático que se origina en el plexo nervioso sacro L4-S3, estimula a su vez los nervios sacros, modulando la función urinaria y defecatoria de forma similar a la neuroestimulación sacra transcutánea.86 - 88
Existen datos pediátricos que respaldan el uso de la ENTP para el EF. Se realizó un estudio prospectivo de 21 niños de 4 a 14 años con EF, diagnosticados según criterios de Roma IV, que recibieron sesiones diarias de 30 minutos de ETNTP durante 10 días en un período de 2 semanas.89 Se observó una mejora significativa en la consistencia de las deposiciones, en la incontinencia fecal y en la presencia e intensidad del dolor abdominal.89
Se publicaron datos alentadores sobre eficacia y seguridad tras la finalización de un ensayo clínico aleatorizado con 82 niños de 4 a 14 años con EF refractario según los criterios de Roma IV.90 Los niños fueron asignados aleatoriamente a 4 semanas de terapia con EPNTP (dos veces al día, administración de corriente de 15 minutos) o a un grupo control (electrodos aplicados sin corriente). A las 12 semanas del inicio de la intervención se logró la remisión clínica en el 78,6 % de los niños que recibieron EPNTP, en comparación con el 38,1% del grupo control.90
Neuroestimulación transcutánea sacra
Es un método no invasivo, de bajo costo, bien tolerado y sin efectos adversos de importancia.91
Los hospitales Profesor Alejandro Posadas y Sor María Ludovica de Argentina practican esta técnica. Los primeros resultados se presentaron en el Congreso mundial de Neurogastroenterología y motilidad pediátrica en Amsterdam, en septiembre de 2025.
En este trabajo fueron tratados 59 pacientes; 25 con diagnóstico de MMC, 17 de MAR y 17 con EF refractario. Se realizaron 12 sesiones semanales de electroestimulación de 30 minutos con dos electrodos posteriores cutáneos entre S2/S4 (Figura 7), y manometría anorrectal antes y después del tratamiento. En relación a la configuración del estimulador: el tiempo de sesión fue de 30 minutos, modo TENS, frecuencia: 25 Hz, ancho de pulso: 200 microsegundos y frecuencia de Burst: 4 Hz. El 56% de los pacientes logró la continencia total, el 29% parcial y el 15% no presentó mejoría. El 31,3% suspendió los laxantes postratamiento, el 30,4% resolvió la incontinencia urinaria y el 22,7% suspendió el cateterismo vesical. Los hallazgos manométricos fueron: mejoría significativa de la presión de reposo, de la contracción voluntaria y de la sensorialidad. El test de calidad de vida realizado antes y después del tratamiento demostró mejoría más evidente en los pacientes con MMC.
Figura 7. Neuroestimulación transuctánea sacra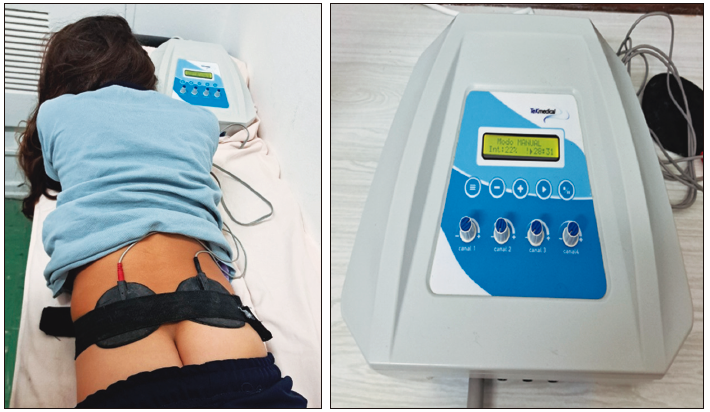
Estimulación eléctrica transcutánea abdominal
La estimulación eléctrica transcutánea abdominal (EET) utiliza un dispositivo compuesto por un generador de voltaje de pulso eléctrico, un cable de interconexión y electrodos que se adhieren a la piel (Figura 6). Administra una corriente interferencial sobre las regiones abdominal y lumbar. La corriente generada puede superar la impedancia de la piel para alcanzar un punto de interés.92 El mecanismo preciso que media el efecto aún no está establecido. Una hipótesis es que produce neuromodulación afectando el movimiento intestinal y la sensibilidad.93
Se colocan dos electrodos en la piel de la pared abdominal a la altura del ombligo y otros dos en la espalda, entre T9 y L2 a cada lado,94 calibrados con una frecuencia de 4 kHz, frecuencia de latido 80 a 160 Hz y corriente < 33 mA.95 La evidencia sobre su eficacia es aún contradictoria93, 96, 97 e insuficiente en pediatría para sacar conclusiones.
Diversos estudios demostraron que la EET en niños con tránsito lento mejoró la frecuencia de la defecación, la incontinencia urinaria, el dolor abdominal, la urgencia defecatoria y la calidad de vida.98 Las complicaciones reportadas son menores, como dolor local.80, 97 - 99
Cirugía
Las cirugías más utilizadas en pacientes con estreñimiento refractario son la derivación colónica con colostomía o ileostomía y, en los casos más graves, la resección colónica parcial. Son intervenciones quirúrgicas mayores que pueden presentar complicaciones importantes y, en algunos casos, beneficios limitados. No siempre se logra abandonar el uso de laxantes.100 Se ha realizado el intento de abordaje trans anal, sin buenos resultados.101-102 Las intervenciones quirúrgicas se ven influenciadas por los resultados de una biopsia rectal, los estudios de tránsito intestinal, la presencia de megacolon/megarrecto en el enema de contraste, el grado de suciedad/incontinencia, los hallazgos de la manometría anorrectal y la evaluación de la motilidad colónica. Por tales motivos, la decisión sobre cuál es la técnica indicada para cada paciente debe ser individualizada.103 Los procedimientos quirúrgicos deben ser la última opción, luego de haber intentado previamente otras terapias disponibles.104
Direcciones futuras en el abordaje terapéutico
Terapia magnética de neuroestimulación translumbosacra
Consiste en la estimulación magnética indolora de los nervios que regulan los músculos del ano y del recto.
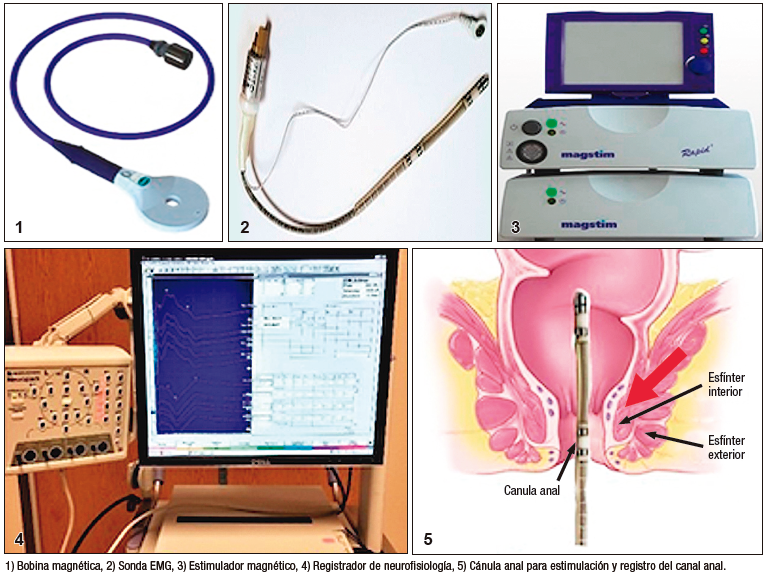
La técnica consiste en colocar una sonda en el recto, que contiene dos pares de electrodos bipolares de anillo de acero (Gaeltec Devices Ltd, Dunvegan®, Escocia) separados por 1 cm. El par distal de electrodos queda ubicado en el canal anal a 1 - 2 cm del borde anal, y el par proximal en el recto, a 9 - 10 cm del borde anal. Además, se colocan 3 electrodos de superficie en el músculo tibial anterior como control. Las estimulaciones magnéticas se realizan utilizando una bobina circular, en la región lumbar y sacra, a unos 4 cm a ambos lados de la línea media (Figura 8).105 Se están realizando estudios en poblaciones adultas que investigan la eficacia de esta tecnología para la incontinencia fecal, con la posibilidad de explorar también su uso en el futuro para el estreñimiento. Existen estudios en población adulta que muestran una mejora significativa de la incontinencia fecal a corto plazo, así como una mejora de la neuropatía, la sensorialidad y la distensibilidad rectal.106 La desventaja de esta tecnología es el uso de una sonda anorrectal, ya que puede existir mayor resistencia a su utilización en poblaciones pediátricas.
Figura 8. Sistema de estimulación magnética anorrectal translumbosacra105
Cápsula vibratoria
La cápsula vibratoria es un dispositivo programable de administración oral que obtuvo la aprobación de la FDA para adultos con estreñimiento crónico en el año 2022 (Figura 9). El mecanismo de acción hipotético es que la cápsula tiene un movimiento vibrante que estimula de manera mecánica la pared intestinal, aumentando el ritmo circadiano de la actividad contráctil colónica, lo que resulta en un aumento de las deposiciones espontáneas.4, 107 Existen múltiples ensayos controlados aleatorizados en adultos con estreñimiento crónico con resultados alentadores que demuestran eficacia y seguridad.108 Actualmente no existen estudios pediátricos centrados en esta tecnología.
Figura 9. Cápsula vibrante
Hipnosis
En un modelo biopsicosocial reconocemos la importancia de los procesos neurobiológicos en las interacciones cerebro-intestino, que conducen a alteraciones en la motilidad, la sensibilidad y las funciones inmunitarias.109 Los mecanismos subyacentes al impacto de la hipnosis en los problemas gastrointestinales aún no están claros, pero los hallazgos de varios estudios sugieren que involucran tanto la modulación del funcionamiento intestinal como cambios en el manejo cerebral de las señales sensoriales del tracto gastrointestinal.110
Los factores psicológicos desempeñan un papel importante en la aparición y el mantenimiento de los trastornos digestivos funcionales, entre ellos el EF.
Los tratamientos médicos, tal como hemos nombrado anteriormente, muchas veces no son suficientes. Esto lleva a prestar más atención a un enfoque no farmacológico que identifique los mecanismos neurobiológicos del binomio mente-cuerpo, como son: yoga, meditación, terapia cognitivo-conductual e hipnosis.111 Si bien tratamientos psicológicos como la terapia cognitivo-conductual y la hipnoterapia han demostrado ser eficaces, integrarlos en la atención médica tradicional es un desafío. Necesitamos eliminar prejuicios tanto del médico como del niño y su familia.111
La hipnoterapia puede permitir la modificación de la comunicación alterada entre el intestino y el cerebro.112 Sin embargo, se requieren más estudios en pacientes pediátricos con EF para poder hacer una recomendación.
El EF y la incontinencia fecal en pediatría son un problema frecuente. Un gran porcentaje de niños persiste sintomático después de 6 a 12 meses de tratamiento; algunos hasta la adolescencia o la edad adulta.113-115 Por lo tanto, es necesario desarrollar e investigar nuevas opciones terapéuticas.
Existen diversas terapias disponibles y en investigación para el estreñimiento refractario en pediatría. Una limitación importante es que gran parte de los datos actuales se refieren a poblaciones adultas y la fisiopatología del estreñimiento en los niños es diferente a la de los adultos. Esto explica por qué ciertos tratamientos muestran excelentes resultados en adultos a diferencia de lo que se observa en pediatría, y viceversa. Se requieren más estudios en poblaciones pediátricas, comparando tanto las distintas terapias entre sí como la respuesta en las diferentes causas (EF, MMC o MAR). A mayor variedad de alternativas terapéuticas, aumenta la posibilidad de realizar un tratamiento personalizado de cada paciente según su fisiopatología y respuesta.
Un factor crucial para el éxito del tratamiento es la adherencia al mismo. La mala adherencia al tratamiento farmacológico de mantenimiento es común en niños y constituye un factor importante en la respuesta.116-118
Las molestias, la insatisfacción con los resultados y el impacto emocional de los síntomas de estreñimiento en el niño son factores que pueden afectar negativamente al resultado del tratamiento.119 Por eso es tan importante contar con diversas opciones y ofrecer un tratamiento individualizado.
Propiedad intelectual. Los autores declaran que los datos, las figuras y las tablas presentes en el manuscrito son originales y se realizaron en sus instituciones pertenecientes. Asimismo, solicitaron autorización y dieron reconocimiento al autor original de las Figuras 1-4, 6 y 8.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflictos de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor

© 2026 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Zubiri C, Zosi A y Bigliardi R Avances en el tratamiento del estreñimiento refractario pediátrico. Acta Gastroenterol Latinoam. 2026;56(1):41-56. https://doi.org/10.52787/agl.v56i1.576
Correspondencia: Cecilia Zubiri
Correo electrónico: cecizubiri03@hotmail.com
Acta Gastroenterol Latinoam 2026;56(1):41-56