Juan I. Olmos1 ID· John E. Pandolfino2 ID
1Sección de Esófago y Neurogastroenterología. División de Gastroenterología y
hepatología. Hospital de Clínicas “José de San Martín” Universidad de Buenos Aires.
Argentina.
2Kenneth C. Griffin Esophageal Center, División de Gastroenterología y
Hepatología Feinberg School of Medicine, Northwestern University, Chicago,
IL, EE.UU.
Acta Gastroenterol Latinoam 2026;56(1):17-28
Recibido: 01/02/2026 / Aceptado: 06/03/2026 / Publicado online: 31/03/2026 / https://doi.org/10.52787/agl.v56i1.601
Los síntomas esofágicos -incluyendo la disfagia, la pirosis, la regurgitación y el dolor torácico no cardiogénico- se encuentran entre las indicaciones más frecuentes de derivación a gastroenterología. A pesar de su elevada prevalencia, el establecimiento de un diagnóstico etiológico definitivo continúa siendo un desafío clínico relevante, debido a la marcada superposición de perfiles sintomáticos entre la enfermedad por reflujo gastroesofágico, la esofagitis eosinofílica, los trastornos motores esofágicos y los trastornos de la interacción intestino-cerebro. Los paradigmas diagnósticos vigentes se basan, en general, en estrategias secuenciales que con frecuencia comienzan con un tratamiento empírico con inhibidores de la bomba de protones, seguido de una endoscopía digestiva alta y, cuando esta no resulta concluyente, de estudios funcionales esofágicos basados en catéter. Este enfoque se asocia a tiempos diagnósticos prolongados, estudios incompletos por mala tolerancia, demoras en el acceso a centros especializados y un incremento sustancial de los costos sanitarios. Los avances recientes en las tecnologías endoscópicas y funcionales ofrecen la oportunidad de replantear de manera fundamental la evaluación de los síntomas esofágicos. La integración de herramientas de estratificación endoscópica de riesgo -como el Clinical Achalasia Risk Score- junto con la planimetría mediante Functional Lumen Imaging Probe y el monitoreo inalámbrico del pH, permite realizar una evaluación fisiológica integral durante la endoscopía índice, bajo sedación, optimizando el rendimiento diagnóstico del procedimiento. Esta estrategia tiene el potencial de reducir significativamente la incertidumbre diagnóstica, acortar el tiempo hasta el diagnóstico definitivo y disminuir la dependencia de estudios con catéter mal tolerados. En esta revisión se sintetiza la evidencia emergente que respalda un paradigma diagnóstico centrado en la endoscopía índice como evento diagnóstico central e integrador. Se analizan las limitaciones de los métodos diagnósticos tradicionales, se revisan los principios fisiológicos y la utilidad clínica de la planimetría mediante Functional Lumen Imaging Probe y el monitoreo inalámbrico de reflujo. Se propone un algoritmo práctico que integra esas herramientas, con el objetivo de brindar una atención de precisión y eficiente, orientada a mejorar el rendimiento diagnóstico y la toma de decisiones terapéuticas en los pacientes con síntomas esofágicos. Dado que la evidencia disponible es emergente y se concentra en centros con experiencia, el algoritmo propuesto debe interpretarse como un marco pragmático para optimizar la secuencia diagnóstica, sujeto a validación prospectiva y adaptación al contexto local.
Palabras claves. Endoscopía índice, planimetría FLIP, trastornos motores esofágicos, monitoreo inalámbrico del pH, Clinical Achalasia Risk Score, enfermedad por reflujo gastroesofágico, esofagitis eosinofílica, unión esofagogástrica, manometría de alta resolución, disfagia.
Esophageal symptoms -including dysphagia, heartburn, regurgitation, and non-cardiogenic chest pain- are among the most common indications for referral to gastroenterology. Despite their high prevalence, establishing a definitive etiological diagnosis remains a significant clinical challenge due to the marked overlap in symptom profiles between gastroesophageal reflux disease, eosinophilic esophagitis, esophageal motility disorders, and disorders of gut–brain interaction. Current diagnostic paradigms are generally based on sequential testing strategies that often begin with empirical treatment with proton pump inhibitor followed by endoscopy and, when this is inconclusive, catheter-based esophageal functional studies. This approach is associated with prolonged diagnostic times, incomplete studies due to poor tolerance, delays in access to specialized centers, and substantial increase in healthcare costs. Recent advances in endoscopic and physiologic technologies offer the opportunity to fundamentally reframe the evaluation of esophageal symptoms. The integration of endoscopic risk stratification tools, such as the Clinical Achalasia Risk Score, Functional Lumen Imaging Probe panometry, and wireless pH monitoring, enables a comprehensive physiologic evaluation during the index endoscopy under sedation, optimizing the diagnostic performance of the procedure. This strategy has the potential to significantly reduce diagnostic uncertainty, shorten the time to definitive diagnosis, and decrease reliance on poorly tolerated catheter studies. This review synthesizes the emerging evidence supporting a diagnostic paradigm centered on index endoscopy as a central and integrative diagnostic event. The limitations of traditional diagnostic methods are analyzed and the physiological principles and clinical utility of planimetry using Functional Lumen Imaging Probe and wireless reflux monitoring are reviewed. A practical algorithm integrating these tools is proposed, with the aim of providing accurate and efficient care, aimed at improving diagnostic performance and therapeutic decision-making in patients with esophageal symptoms. Given that the available evidence is still emerging and concentrated in centers with experience, the proposed algorithm should be interpreted as a pragmatic framework for optimizing the diagnostic sequence, subject to prospective validation and adaptation to the local context.
Keywords. Index endoscopy, FLIP planimetry, esophageal motility disorders, wireless pH monitoring, Clinical Achalasia Risk Score, gastroesophageal reflux disease, eosinophilic esophagitis, esophagogastric junction, high-resolution manometry, dysphagia.
Abreviaturas
ERGE: Enfermedad por reflujo gastroesofágico.
EoE: Esofagitis
eosinofílica.
IBP: Inhibidores de la bomba de protones.
CARS: Clinical Achalasia
Risk Score.
FLIP: Functional Lumen Imaging Probe.
pH: Potencial de
hidrógeno.
MAR: Manometría de alta resolución.
UEG: Unión
esofagogástrica.
EREFS: Edema, Rings (anillos), Exudates (exudados), Furrows (surcos),
Strictures (estenosis).
PIR: Presión integrada de relajación.
DI-UEG: Índice de
distensibilidad de la unión esofagogástrica.
CRA: Contracciones repetitivas
anterógradas.
AET: Acid Exposure Time (tiempo de exposición ácida).
Los síntomas esofágicos, como pirosis, disfagia, regurgitación, dolor torácico e impactación alimentaria, representan una proporción sustancial de las consultas ambulatorias en gastroenterología. Si bien se trata de manifestaciones clínicas frecuentes, las etiologías subyacentes son heterogéneas y, en muchos casos, difíciles de diferenciar basándose únicamente en la historia clínica. La enfermedad por reflujo gastroesofágico (ERGE), la esofagitis eosinofílica (EoE), los trastornos motores esofágicos y los trastornos funcionales del esófago suelen presentarse con perfiles sintomáticos superpuestos. Esto conduce a la ambigüedad diagnóstica y la incertidumbre terapéutica.1
Históricamente, la evaluación de los síntomas esofágicos se ha apoyado en ensayos terapéuticos empíricos, en particular con inhibidores de la bomba de protones (IBP), seguidos de la realización de una endoscopía digestiva alta y, cuando resulta necesario, pruebas funcionales esofágicas. Si bien este modelo se encuentra firmemente incorporado en la práctica clínica habitual, en la actualidad se reconoce de manera creciente que dicho enfoque puede resultar ineficiente desde el punto de vista diagnóstico y poco efectivo para establecer la etiología subyacente de los síntomas en un número significativo de casos. El tratamiento empírico se asocia a un efecto placebo significativo, retrasos en el diagnóstico definitivo y una prolongación innecesaria del malestar del paciente, especialmente en aquellos con trastornos motores esofágicos o trastornos de la interacción intestino-cerebro.2, 3
La endoscopía continúa siendo la piedra angular en la evaluación esofágica debido a su capacidad para excluir malignidad, identificar la enfermedad mucosa y detectar una obstrucción mecánica. Sin embargo, hasta el 50 - 70% de los pacientes sometidos a una endoscopía digestiva alta por síntomas esofágicos no presentan anormalidades evidentes, lo que deja a los clínicos con escasa claridad diagnóstica y a los pacientes con síntomas persistentes.3 En estos casos son necesarias las pruebas funcionales esofágicas -manometría de alta resolución (MAR), monitoreo ambulatorio del reflujo y esofagograma baritado- para establecer un diagnóstico. Lamentablemente, estos estudios suelen realizarse semanas o meses más tarde, requieren derivación a centros especializados y están limitadas por una tolerancia subóptima y una proporción no despreciable de estudios incompletos.2, 3
Actualmente los avances en la evaluación fisiológica endoscópica permiten ir más allá del rol puramente excluyente de patología orgánica de la endoscopía. Durante la endoscopía bajo sedación pueden utilizarse herramientas como la planimetría FLIP y el monitoreo inalámbrico del pH (colocación de la capsula), proporcionando una evaluación en tiempo real de la motilidad esofágica, la dinámica de apertura de la unión esofagogástrica (UEG) y la carga de reflujo. Cuando se combinan con sistemas estructurados de estratificación endoscópica de riesgo, como el Clinical Achalasia Risk Score (CARS),4, 5 estas tecnologías permiten un enfoque diagnóstico de precisión integrado durante la endoscopía índice.
En este contexto, la presente revisión propone un cambio de paradigma en la evaluación de los síntomas esofágicos, posicionando a la endoscopía índice como un evento diagnóstico central e integrador más que como una prueba preliminar de cribado. La integración de la evaluación endoscópica, los estudios fisiológicos y el monitoreo objetivo del reflujo en un mismo estudio, permite reducir las demoras diagnósticas, mejorar la experiencia del paciente y optimizar la toma de decisiones diagnósticas y terapéuticas. Cabe destacar que esta estrategia se apoya en evidencia reciente pero todavía en expansión, por lo que su implementación requiere considerar la disponibilidad tecnológica, el entrenamiento del equipo y los escenarios clínicos específicos.
Limitaciones del paradigma diagnóstico actual
Prolongación de los tiempos diagnósticos
El enfoque diagnóstico tradicional para la evaluación de los síntomas esofágicos es inherentemente secuencial y prolongada. Los pacientes con pirosis o dolor torácico suelen recibir tratamiento empírico con IBP durante 4 - 8 semanas antes de considerar una evaluación adicional. Cuando los síntomas persisten, se realiza una endoscopía digestiva alta y, con frecuencia, se indican estudios de monitoreo de reflujo ambulatorio o manometría si los hallazgos endoscópicos no son concluyentes. Este enfoque escalonado suele dar lugar a tiempos diagnósticos que se extienden de tres a seis meses, y en algunos casos superan el año.2
La disfagia constituye un escenario particularmente ilustrativo de estas limitaciones. Si bien la endoscopía se prioriza de manera apropiada por su rol en la exclusión de patología maligna, un examen endoscópico normal suele dar lugar a la necesidad de evaluaciones adicionales. La acalasia y otros trastornos motores esofágicos son especialmente susceptibles a retrasos diagnósticos, dado que las etapas iniciales de la enfermedad pueden cursar con hallazgos endoscópicos normales o con estudios por imágenes equívocos. Diversos trabajos han demostrado que los pacientes con acalasia experimentan con frecuencia demoras diagnósticas superiores a los 12 meses, período durante el cual los síntomas suelen atribuirse erróneamente a ERGE o a trastornos funcionales.3
Dependencia excesiva del tratamiento empírico
El tratamiento empírico con inhibidores de la bomba de protones (IBP) continúa siendo una estrategia inicial ampliamente utilizada en pacientes con síntomas esofágicos, en particular pirosis y dolor torácico. Si bien este enfoque puede ser apropiado en poblaciones seleccionadas, su aplicación indiscriminada plantea limitaciones relevantes desde el punto de vista diagnóstico. La respuesta clínica a los IBP no permite discriminar de manera confiable entre la enfermedad por reflujo gastroesofágico, la hipersensibilidad al reflujo y la pirosis funcional. La mejoría sintomática observada puede reflejar un efecto placebo más que una modificación de la enfermedad.6 Por el contrario, los pacientes con trastornos motores o EoE pueden experimentar retrasos diagnósticos debido a una respuesta transitoria o ausente a la supresión ácida.
Fragmentación de los estudios y barreras de acceso
Las pruebas funcionales esofágicas son esenciales para el diagnóstico de los trastornos motores y la caracterización de la ERGE pero el acceso a estas pruebas es limitado. La manometría de alta resolución y el monitoreo de pH-impedancia requieren equipamiento específico y personal con entrenamiento especializado, recursos que con frecuencia se concentran en centros terciarios. Como consecuencia, los tiempos de espera para la realización de estos estudios suelen extenderse por varios meses, en particular en ámbitos no académicos o comunitarios. Además, hasta el 20% de los estudios resultan incompletos o fallidos debido a intolerancia, dificultades técnicas o ansiedad del paciente durante la realización de los mismos.2, 3
Experiencia del paciente y tolerancia a los estudios
Los métodos diagnósticos basados en catéter constituyen una barrera importante para una evaluación eficaz. La manometría transnasal y el monitoreo de pH-impedancia se asocian con molestias, náuseas, dolor nasal y ansiedad procedimental. En un estudio prospectivo que evaluó la experiencia del paciente con pruebas diagnósticas esofágicas, la MAR fue el único estudio significativamente asociado con una experiencia traumática (χ² = 8,92; p = 0,003).7 Estos factores contribuyen al rechazo de estudios, pruebas incompletas y retrasos diagnósticos.
Justificación para optimizar la endoscopía índice
Dadas las limitaciones del paradigma actual, existe una sólida justificación para renovar la conceptualización del rol de la endoscopía índice en la evaluación de los síntomas esofágicos. La endoscopía ya es un punto final inevitable para la mayoría de los pacientes debido a síntomas de alarma, enfermedad refractaria o incertidumbre diagnóstica.1 Aprovechar esta endoscopía índice para realizar una evaluación fisiológica bajo sedación ofrece múltiples ventajas.
En primer lugar, la endoscopía proporciona información anatómica y mucosa crítica que contextualiza los hallazgos fisiológicos. La graduación de la esofagitis mediante la clasificación de Los Ángeles, la evaluación de EoE con biopsias sistemáticas y puntuación EREFS, la valoración de la válvula gastroesofágica y de la hernia hiatal, así como la identificación de signos endoscópicos sugestivos de acalasia, aportan elementos fundamentales para la interpretación integrada de los datos fisiológicos posteriores.8
En segundo lugar, la introducción de herramientas estructuradas de estratificación endoscópica de riesgo, como el Clinical Achalasia Risk Score (CARS), permite estimar la probabilidad de acalasia basándose en hallazgos endoscópicos reproducibles. El CARS incorpora la evaluación del contenido esofágico, la anatomía luminal, la resistencia a nivel de la UEG y los cambios mucosos relacionados con estasis, demostrando un excelente valor predictivo para acalasia cuando los puntajes superan los umbrales predefinidos.4, 5
En tercer lugar, la planimetría mediante la tecnología Functional Lumen Imaging Probe (FLIP) permite una evaluación directa de la dinámica de apertura de la UEG y de la respuesta contráctil esofágica durante la endoscopía bajo sedación. A diferencia de la MAR, que evalúa la peristalsis inducida por la deglución, la tecnología FLIP evalúa la peristalsis secundaria inducida por distensión, además de la rigidez de la pared esofágica, proporcionando información fisiológica complementaria particularmente valiosa en pacientes con hallazgos manométricos equívocos o limítrofes.9-12
Por último, la cápsula para el monitoreo inalámbrico del pH puede colocarse durante el mismo procedimiento, permitiendo una evaluación objetiva de la exposición ácida durante 48 - 96 horas sin la incomodidad de los catéteres transnasales. Este enfoque se alinea con las guías contemporáneas de ERGE y facilita una fenotipificación precisa de la ERGE en etapas tempranas del proceso diagnóstico.13, 14
En conjunto, estos avances respaldan la transición hacia una estrategia diagnóstica integral y de precisión, basada en la endoscopía índice como evento diagnóstico central e integrador dentro del abordaje de los síntomas esofágicos.
Hay que considerar, sin embargo, que en Latinoamérica la disponibilidad de planimetría FLIP y de monitoreo inalámbrico prolongado del pH es heterogénea. En este contexto, el enfoque centrado en la endoscopía índice podría implementarse de manera escalonada, priorizando su uso en pacientes con mayor probabilidad pretest de trastornos motores u optimizando la derivación dirigida a centros de referencia.
Evaluación motora endoscópica mediante planimetría FLIP
Bases fisiológicas de la planimetría FLIP
La functional lumen imaging probe (FLIP) fue desarrollada para evaluar las propiedades mecánicas y neuromusculares del esófago mediante planimetría por impedancia durante la distensión volumétrica controlada. A diferencia de la manometría de alta resolución (MAR), que evalúa los patrones de presión generados por la peristalsis primaria inducida por la deglución, la planimetría FLIP evalúa la respuesta esofágica a la distensión sostenida, evaluando así la peristalsis secundaria y la rigidez de la pared esofágica.
Durante la planimetría FLIP, un catéter con balón complaciente que contiene múltiples electrodos de impedancia y un transductor de presión se posiciona atravesando la unión esofagogástrica (UEG). La distensión escalonada o sostenida del balón (habitualmente 40 - 70 mL) genera una deformación luminal que permite la medición simultánea del área transversal y la presión intrabalón a lo largo del eje esofágico. Los datos se representan como mapas espaciotemporales de diámetro, proporcionando una visualización en tiempo real de la apertura de la UEG y de la actividad contráctil del cuerpo esofágico.12
Este enfoque ofrece varias ventajas fisiológicas. La distensión luminal activa reflejos entéricos intrínsecos, independientes de los mecanismos centrales de la deglución, lo que permite evaluar la integridad neuromiogénica incluso en pacientes incapaces de generar degluciones confiables. Además, las contracciones inducidas por distensión siguen el gradiente de latencia intrínseco del esófago, evidenciando alteraciones clínicamente relevantes en la coordinación, propagación y vigor contráctil que pueden no ser evidentes en la MAR.9-11
Evaluación de la dinámica de apertura de la unión esofagogástrica
Una fortaleza clave de la planimetría FLIP es su capacidad para cuantificar la dinámica de apertura de la UEG. Las métricas manométricas tradicionales, como la presión integrada de relajación (IRP), infieren la relajación de la UEG basándose en la presión intraluminal durante la deglución. En contraste, la FLIP mide directamente la apertura mecánica de la UEG bajo distensión, integrando de forma simultánea los efectos del tono del esfínter esofágico inferior, la función del diafragma crural y la complacencia de la pared esofágica.
La apertura de la UEG se evalúa mediante dos parámetros principales: el índice de distensibilidad de la UEG (DI-UEG), calculado como el área transversal mínima dividida por la presión intrabalón, y el diámetro máximo de la UEG alcanzado durante la distensión. Estas métricas han sido validadas frente al esofagograma baritado cronometrado y en relación con resultados clínicos, demostrando asociaciones sólidas con la obstrucción clínicamente relevante.9, 11
Según los umbrales establecidos, la apertura de la UEG puede categorizarse como normal, limítrofe o reducida. La apertura normal se define por un DI-UEG ≥ 2,0 mm²/mmHg con un diámetro máximo ≥ 16 mm, mientras que la apertura reducida se define por un DI-UEG < 2,0 mm²/mmHg con un diámetro máximo < 12 mm. La apertura limítrofe incluye valores intermedios que no cumplen criterios para ninguna de las dos categorías.12
Es fundamental interpretar la apertura de la UEG en el contexto de la respuesta contráctil esofágica. Una UEG mecánicamente adecuada puede, no obstante, generar obstrucción funcional del tránsito del bolo en pacientes con peristalsis ausente o gravemente deteriorada, lo que subraya la necesidad de una interpretación integrada y contextualizada, en lugar de basarse en métricas aisladas.
Patrones de respuesta contráctil en la planimetría FLIP
La planimetría FLIP permite clasificar la respuesta contráctil del esófago a la distensión en patrones reproducibles que se correlacionan con fenotipos motores clínicamente relevantes. La respuesta contráctil normal se define por la presencia de contracciones repetitivas anterógradas (CRA), que cumplen la “regla de los 6”: al menos seis contracciones anterógradas consecutivas que se extienden ≥ 6 cm en longitud axial, a una frecuencia de 6 ± 3 contracciones por minuto.10, 12
La respuesta contráctil limítrofe se caracteriza por contracciones anterógradas distinguibles que no cumplen completamente los criterios de CRA, mientras que la respuesta deteriorada o desorganizada refleja una actividad contráctil ausente o irregular sin propagación organizada. La respuesta contráctil ausente denota la falta completa de contracción del cuerpo esofágico durante la distensión.
Una categoría distintiva, denominada respuesta contráctil espástica-reactiva, incluye contracciones oclusivas sostenidas, contracción sostenida del esfínter esofágico inferior o contracciones repetitivas retrógradas. Este patrón se asocia fuertemente con trastornos motores espásticos, incluyendo la acalasia tipo III, el espasmo esofágico distal y el esófago hipercontráctil (Jackhammer).12
Estos fenotipos basados en FLIP muestran una concordancia sustancial con los diagnósticos de la Clasificación de Chicago v4.0, al tiempo que proporcionan información complementaria, particularmente en casos con hallazgos manométricos equívocos o estudios manométricos incompletos.
Integración de la planimetría FLIP con la estratificación endoscópica de riesgo
Rol del Clinical Achalasia Risk Score (CARS)
Si bien la planimetría FLIP proporciona datos fisiológicos robustos, su poder diagnóstico se ve potenciado cuando se interpreta junto con una estratificación endoscópica del riesgo estructurada. El Clinical Achalasia Risk Score (CARS) fue desarrollado para abordar el retraso diagnóstico persistente asociado a la acalasia, mediante la cuantificación de características endoscópicas vinculadas a la obstrucción del flujo esofágico.9
El CARS incorpora cuatro dominios: contenido esofágico, anatomía luminal, resistencia a nivel de la UEG y cambios mucosos relacionados con estasis. Los puntajes varían de 0 a 8 y los valores más altos indican una mayor probabilidad de acalasia. Los estudios de validación han demostrado que un puntaje CARS > 4 confiere una probabilidad superior al 95% de acalasia, mientras que puntajes de 0 – 1 se asocian con una probabilidad muy baja de la enfermedad.4
Diagnóstico basado en probabilidad mediante CARS y FLIP
La integración del CARS con la planimetría FLIP permite un marco diagnóstico basado en probabilidades que trasciende la clasificación binaria. Los pacientes con puntajes CARS elevados y apertura reducida de la UEG en la FLIP presentan una probabilidad extremadamente alta de acalasia y pueden avanzar directamente hacia un tratamiento definitivo sin necesidad de manometría confirmatoria. Este enfoque es particularmente relevante para aquellos pacientes con patrones clásicos de obstrucción no espástica, donde la certeza diagnóstica es elevada. Sin embargo, hay que considerar que esta conducta debería reservarse para los escenarios con probabilidad pretest muy alta, concordancia clínico-endoscópica-fisiológica y disponibilidad de un equipo con experiencia, dado que la manometría de alta resolución continúa siendo el estándar de referencia para la clasificación motora formal y para la definición terapéutica en los fenotipos intermedios o discordantes.
Por el contrario, los pacientes con puntajes CARS bajos y apertura normal de la UEG con respuesta contráctil preservada o limítrofe tienen escasa probabilidad de presentar un trastorno motor mayor. En estos casos, la evaluación debería orientarse hacia la ERGE o los trastornos de la interacción intestino–cerebro, en lugar de realizar estudios adicionales de motilidad.
Los escenarios intermedios -como la apertura limítrofe de la UEG, los patrones contráctiles espásticos-reactivos o los puntajes CARS moderados- identifican a los pacientes que más se benefician de la MAR o del esofagograma baritado cronometrado. Cabe destacar que los estudios sugieren que solo el 30 al 50% de los pacientes en este grupo intermedio cumplen finalmente criterios para un trastorno motor mayor, lo que resalta el valor de una indicación dirigida de estos estudios, en lugar de su uso rutinario.5
En el paradigma propuesto, centrado en la endoscopía índice con planimetría FLIP, el esofagograma debe reservarse para los casos equívocos de sospecha de obstrucción, en particular cuando persiste la incertidumbre diagnóstica tras la FLIP o cuando existe discordancia entre la FLIP y la manometría de alta resolución. En pacientes con acalasia manifiesta y puntajes CARS elevados, la evaluación radiológica rara vez modifica la conducta. No obstante, el tránsito esofágico baritado -particularmente cuando se realiza con el protocolo cronometrado y tableta- continúa teniendo utilidad clínica en la evaluación del tránsito del bolo, la repercusión funcional de la obstrucción y la correlación con la sintomatología, especialmente en aquellos escenarios de disfagia intermitente o cuando se requiere una apreciación dinámica complementaria.
En conjunto, este enfoque integrado permitiría reducir de manera sustancial la necesidad de estudios con catéter, preservando al mismo tiempo una elevada precisión diagnóstica.
Monitoreo inalámbrico del pH durante la endoscopía índice
Fundamentación y consideraciones técnicas
El monitoreo inalámbrico del pH fue desarrollado con el objetivo de superar las limitaciones de tolerancia asociadas a los estudios de reflujo con catéter transnasal. La cápsula se fija endoscópicamente al esófago distal, habitualmente a 6 cm por encima de la unión escamocolumnar, y permite registrar la exposición ácida esofágica durante 48 a 96 horas. Este período prolongado de monitoreo mejora el rendimiento diagnóstico al capturar la variabilidad diaria de los patrones de reflujo.14
Un aspecto particularmente relevante es que el monitoreo inalámbrico del pH puede realizarse durante la misma endoscopía en la que se efectúa la planimetría FLIP, evitando la necesidad de procedimientos adicionales. Esta característica resulta especialmente ventajosa en los pacientes evaluados sin inhibidores de la bomba de protones, como recomiendan las guías contemporáneas cuando el diagnóstico de ERGE es incierto.6
Rol en la fenotipificación de la ERGE y los trastornos funcionales
La evaluación objetiva del reflujo es fundamental para diferenciar la ERGE patológica de la hipersensibilidad al reflujo y la pirosis funcional. La respuesta sintomática a los IBP, por sí sola, no resulta suficiente para establecer un diagnóstico etiológico, dado que el efecto placebo y los mecanismos no ácidos contribuyen de manera significativa a la percepción de los síntomas.
El monitoreo inalámbrico del pH permite una cuantificación precisa del tiempo de exposición ácida (acid exposure time, AET) y facilita la correlación con los eventos sintomáticos reportados por el paciente. De acuerdo con el Consenso de Lyon 2.0, un AET patológico (> 6%) es una evidencia concluyente de ERGE, mientras que un AET normal (< 4%) permite excluir de manera confiable la enfermedad mediada por ácido.14 Los valores intermedios requieren una interpretación contextual, apoyada en métricas adicionales o en la correlación clínica.
Cuando se integra con la planimetría FLIP y la evaluación endoscópica, el monitoreo inalámbrico del pH permite una fenotipificación integral de los pacientes con síntomas esofágicos. Aquellos con apertura normal de la unión esofagogástrica, motilidad conservada y exposición ácida normal se clasifican con mayor precisión dentro del espectro de los trastornos de la interacción intestino-cerebro, lo que orienta el manejo hacia neuromoduladores, terapia conductual y estrategias de reaseguro, en lugar de intensificar la supresión ácida.
En este contexto, un estudio reciente realizado en Latinoamérica demostró que el monitoreo inalámbrico prolongado del pH permite reclasificar más del 70% de los pacientes con AET limítrofe en estudios de pH-impedancia de 24 horas, superando la “zona gris” diagnóstica asociada a los métodos con catéter, que continúan siendo los más utilizados en la región por limitaciones de acceso y costo.17
Impacto clínico de una estrategia integrada centrada en la endoscopía índice
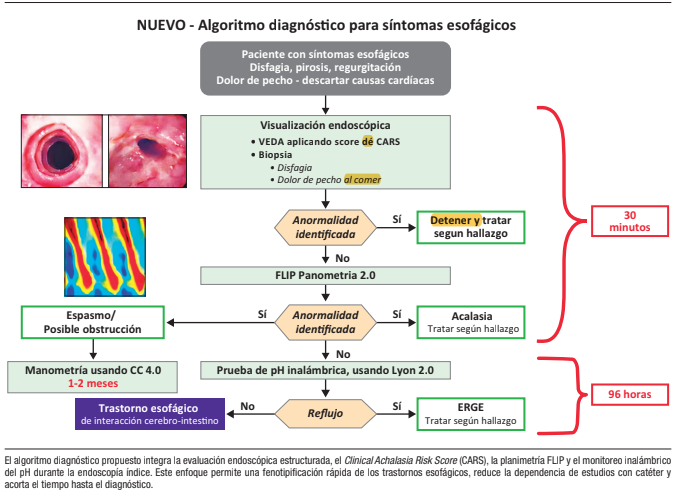
Al incorporar la planimetría FLIP, la puntuación CARS y el monitoreo inalámbrico del pH en la endoscopía índice, los clínicos pueden establecer un diagnóstico definitivo en la mayoría de los pacientes que, de otro modo, tendrían una evaluación inconclusa. En los pacientes restantes, los datos fisiológicos obtenidos durante la endoscopía permiten una selección dirigida de pruebas confirmatorias. En series recientes de centros con experiencia se ha observado que permitieron reducir la indicación de manometría en una proporción sustancial de pacientes y acortar el tiempo diagnóstico, aunque la magnitud de estos beneficios puede variar según el circuito asistencial local. (Figura 1). Si bien los datos disponibles sugieren beneficios clínicos y de eficiencia, la magnitud del impacto puede variar según el acceso local a FLIP, al monitoreo inalámbrico de pH y la experiencia en la interpretación fisiológica.
Esta estrategia se alinea con datos emergentes de costo-efectividad que demuestran que la evaluación fisiológica temprana es clínicamente superior y económicamente ventajosa en comparación con el tratamiento empírico y los diagnósticos diferidos.15, 16 Además, la realización de estas evaluaciones bajo sedación mejora notablemente la experiencia del paciente y las tasas de finalización de los estudios.
Algoritmo diagnóstico pragmático centrado en la endoscopía índice
La Figura 2 presenta un algoritmo diagnóstico propuesto que reposiciona la endoscopía índice como el evento diagnóstico central para los pacientes que consultan por síntomas esofágicos. Este enfoque parte del reconocimiento de que la endoscopía digestiva alta resulta inevitable en la mayoría de los casos, ya sea por la presencia de síntomas de alarma, refractariedad al tratamiento empírico o persistente incertidumbre diagnóstica, y se aprovecha esta instancia para incorporar una evaluación fisiológica integral.
Figura 1. Algoritmo diagnóstico centrado en la endoscopía índice
Figura 2. Aplicación clínica combinada del CARS y planimetría FLIP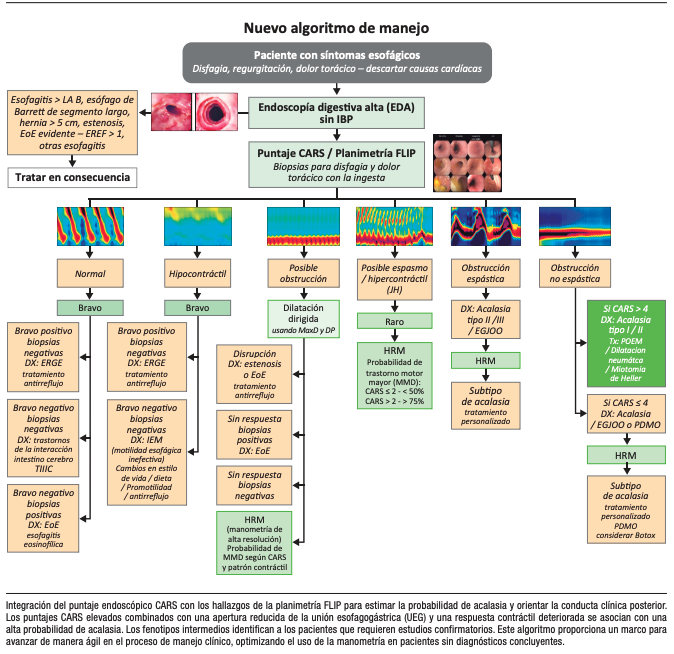
Los pacientes que presentan disfagia, regurgitación, dolor torácico relacionado con la ingesta o pirosis refractaria se someten a una endoscopía digestiva alta de alta calidad, idealmente sin IBP cuando resulta factible. La evaluación endoscópica incluye la valoración sistemática de enfermedad mucosa (clasificación de Los Ángeles y puntuación EREFS), la exclusión de obstrucción mecánica, la identificación de anomalías anatómicas -como hernia hiatal mediante la clasificación de Hill- y la evaluación de hallazgos sugestivos de acalasia mediante el Clinical Achalasia Risk Score (CARS).
Cuando se identifica una etiología evidente -como esofagitis grado B o superior según la clasificación de Los Ángeles, esofagitis eosinofílica con confirmación histológica, estenosis fija, malignidad o hernia hiatal de gran tamaño- el manejo continúa de acuerdo con el diagnóstico establecido, sin necesidad de pruebas fisiológicas adicionales. Sin embargo, en ausencia de una etiología clara, se realiza una planimetría FLIP durante la misma sesión endoscópica.
La planimetría FLIP estratifica a los pacientes según la dinámica de apertura de la UEG y la respuesta contráctil. Los pacientes con apertura reducida de la UEG y respuesta contráctil deteriorada o ausente, particularmente en el contexto de un puntaje CARS elevado, presentan una alta probabilidad de presentar acalasia, y podrían avanzar directamente a un tratamiento definitivo sin necesidad de manometría confirmatoria. En contraste, los pacientes con patrones contráctiles espásticos-reactivos podrían ser derivados a manometría de alta resolución para definir el subtipo y guiar una estrategia terapéutica personalizada.
Los pacientes con apertura normal de la UEG y respuesta contráctil preservada o limítrofe presentan una baja probabilidad de presentar un trastorno motor mayor. En estos casos, el monitoreo inalámbrico del pH realizado durante la endoscopía índice permite una fenotipificación precisa de la ERGE. Una exposición ácida patológica respalda el diagnóstico de ERGE y orienta el tratamiento con supresión ácida o intervenciones antirreflujo, mientras que una exposición ácida normal favorece el diagnóstico de un trastorno de la interacción intestino-cerebro y dirige el manejo hacia la neuromodulación, intervenciones conductuales y estrategias de reaseguro.
Este algoritmo permite establecer un diagnóstico definitivo en pocos días para la mayoría de los pacientes, minimizando los retrasos diagnósticos y reduciendo la dependencia de pruebas con catéter mal toleradas.
Al consolidar las pruebas diagnósticas en una única instancia, el algoritmo propuesto reduce la redundancia procedimental, acorta el tiempo hasta el tratamiento y mejora la satisfacción del paciente. Estos beneficios son especialmente relevantes para los sistemas de salud, que enfrentan una demanda creciente, acceso limitado a pruebas subespecializadas y presión para reducir las prácticas de bajo valor clínico.
Figura 3. Aplicación clínica basada en la integración del CARS y la planimetría FLIP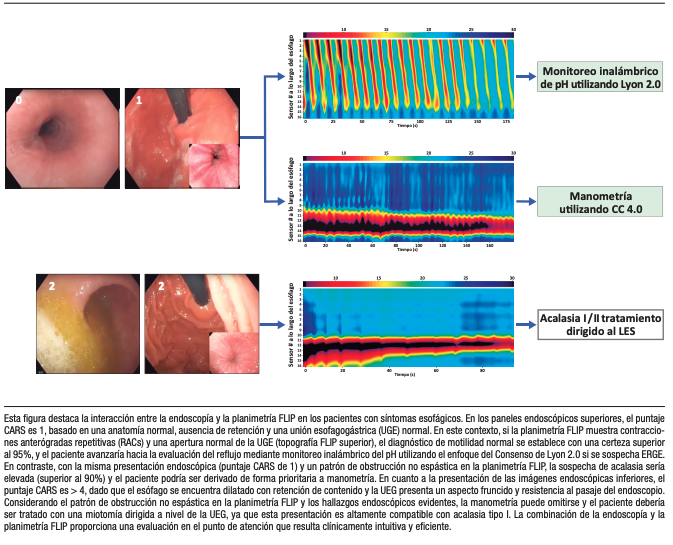
Figura 4.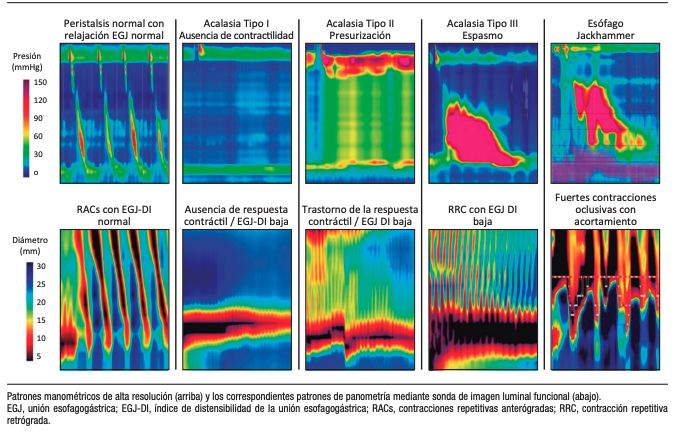
Direcciones futuras
La integración de la planimetría FLIP y la evaluación endoscópica estructurada representa solo el primer paso hacia una esofagología de precisión. Las investigaciones actuales apuntan a mejorar la caracterización fisiológica del esófago mediante la incorporación de mediciones cuantitativas del trabajo esofágico y la potencia contráctil, que reflejan cuánta energía genera el órgano para propulsar el bolo, superando así la evaluación basada únicamente en la presión o el diámetro.
La inteligencia artificial y el aprendizaje automático ofrecen vías prometedoras para mejorar la precisión diagnóstica y la reproducibilidad. La interpretación automatizada de los hallazgos endoscópicos, la puntuación CARS y los patrones de planimetría FLIP podría constituir un soporte decisional en tiempo real durante la endoscopía, reduciendo la dependencia del operador y facilitando una adopción más amplia de estos recursos diagnósticos. Trabajos iniciales que utilizan modelos matemáticos simplificados y simulaciones computacionales del esófago sugieren que la combinación de datos fisiológicos con modelado computacional podría permitir una mayor personalización del tratamiento, especialmente en los trastornos motores complejos.
Se requieren estudios prospectivos futuros para validar los umbrales basados en resultados clínicos para la planimetría FLIP, evaluar los resultados clínicos a largo plazo de los algoritmos centrados en la endoscopía índice y definir opciones terapéuticas óptimas para fenotipos intermedios. A medida que estos datos emerjan, es probable que el rol de la endoscopía en la enfermedad esofágica evolucione de una herramienta puramente diagnóstica a una plataforma para la evaluación fisiológica integrada y la toma de decisiones terapéuticas.
Propiedad intelectual. Los autores declaran que los datos y las figuras presentes en el manuscrito son originales y se realizaron en sus instituciones pertenecientes.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflictos de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor

© 2026 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Olmos J I y Pandolfino J E. Redefiniendo la evaluación endoscópica inicial de los síntomas esofágicos: hacia un paradigma diagnóstico basado en la precisión. Acta Gastroenterol Latinoam. 2026;56(1):17-28. https://doi.org/10.52787/agl.v56i1.601
Correspondencia: Juan Ignacio Olmos
Correo electrónico: juan.ignacio.olmos@gmail.com
Acta Gastroenterol Latinoam 2026;56(1):17-28